Rýchlotestovacia kazeta na antigén SARS-CoV-2
Stručný popis:
Kazetový rýchly test na antigén SARS-CoV-2 je rýchly chromatografický imunotest na kvalitatívnu detekciu antigénu SARS-CoV-2 v ľudských orofaryngeálnych výteroch. Identifikácia je založená na monoklonálnych protilátkach špecifických pre nukleokapsidový (N) proteín SARS-CoV-2. Je určený na pomoc pri rýchlej diferenciálnej diagnostike infekcie COVID-19.
URČENÉ POUŽITIE
Ten/Tá/ToRýchlotestovacia kazeta na antigén SARS-CoV-2je rýchly chromatografický imunotest na kvalitatívnu detekciu antigénu SARS-CoV-2 v ľudských orofaryngeálnych výteroch. Identifikácia je založená na monoklonálnych protilátkach špecifických pre nukleokapsidový (N) proteín SARS-CoV-2. Je určený na pomoc pri rýchlej diferenciálnej diagnostike...COVID-19infekcia.
Špecifikácie balenia
25 testov/balenie, 50 testov/balenie, 100 testov/balenie
ÚVOD
Nové koronavírusy patria do rodu β.COVID-19je akútne respiračné infekčné ochorenie. Ľudia sú vo všeobecnosti náchylní. V súčasnosti sú pacienti infikovaní novým koronavírusom hlavným zdrojom infekcie; asymptomatickí infikovaní ľudia môžu byť tiež zdrojom infekcie. Na základe súčasného epidemiologického výskumu je inkubačná doba 1 až 14 dní, väčšinou 3 až 7 dní. Medzi hlavné prejavy patrí horúčka, únava a suchý kašeľ. V niekoľkých prípadoch sa vyskytuje upchatý nos, nádcha, bolesť hrdla, bolesti svalov a hnačka.
REAGENTY
Testovacia kazeta obsahuje častice nukleokapsidového proteínu anti-SARS-CoV-2 a nukleokapsidový proteín anti-SARS-CoV-2 potiahnutý na membráne.
PREVENCIA
Pred vykonaním testu si prečítajte všetky informácie v tomto príbalovom letáku.
1. Len na profesionálne diagnostické použitie in vitro. Nepoužívajte po dátume exspirácie.
2. Test by mal zostať v uzavretom vrecku až do použitia.
3. Všetky vzorky by sa mali považovať za potenciálne nebezpečné a mali by sa s nimi zaobchádzať rovnako ako s infekčným agensom.
4. Použitý test by sa mal zlikvidovať v súlade s miestnymi predpismi.
5. Vyhnite sa používaniu krvavých vzoriek.
6. Pri manipulácii so vzorkami noste rukavice, nedotýkajte sa membrány činidla a nádobky na vzorku.
SKLADOVANIE A STABILITA
Doba použiteľnosti je 18 mesiacov, ak je tento výrobok skladovaný v prostredí
2 – 30 ℃. Test je stabilný do dátumu exspirácie uvedeného na zatavenom vrecku. Test musí zostať v zatavenom vrecku až do použitia.NEZMRAZUJTE.Nepoužívajte po dátume spotreby.
ODBER A PRÍPRAVA VZORIEK
1. Odber sekrétu z hrdla: Sterilný tampón vložte do hrdla úplne z úst, pričom stred zamerajte na stenu hrdla a začervenanú oblasť podnebných mandlí, utrite obojstranné faryngeálne mandle a zadnú stenu hltana miernym prúdom vody.
silou, nedotýkajte sa jazyka a vyberte tampón.
2. Vzorku ihneď po odbere spracujte roztokom na extrakciu vzorky, ktorý je súčasťou súpravy. Ak ju nie je možné spracovať ihneď, vzorka by sa mala uchovávať v suchej, sterilizovanej a prísne uzavretej plastovej skúmavke. Môže sa skladovať pri teplote 2 – 8 ℃ počas 8 hodín a pri teplote –70 ℃ môže byť dlhodobo skladovaná.
3. Vzorky silne kontaminované zvyškami jedla z ústnej dutiny sa nemôžu použiť na testovanie tohto produktu. Vzorky odobraté z tampónov, ktoré sú príliš viskózne alebo zhlukované, sa na testovanie tohto produktu neodporúčajú. Ak sú tampóny kontaminované veľkým množstvom krvi, neodporúčajú sa na testovanie. Neodporúča sa používať na testovanie tohto produktu vzorky spracované roztokom na extrakciu vzoriek, ktorý nie je súčasťou tejto súpravy.
KOMPONENTY SÚPRAVY
Materiály poskytujú
| Testovacie kazety | Extrakčné činidlo | Extrakčné trubice | |
| Sterilné tampóny | Príbalový leták | Pracovná stanica |
Materiály potrebné, ale neposkytnuté
| Časovač | Na meranie času. |
| Balík |
Špecifikácie25
testy/balenie50
testy/balenie100
Extrakcia vzorky - činidlo 25 testov/balenie 50 testov/balenie 100 testov/balenie Extrakcia vzorky
skúmavka ≥25 testov/balenie ≥50 testov/balenie ≥100 testov/balenie Pokyny Pozrite si
balíkPozrite si
balíkPozrite si
balík
NÁVOD NA POUŽITIE
Pred testovaním nechajte testovaný materiál, vzorku a extrakčný pufor vychladnúť na izbovú teplotu (15 – 30 ℃).
1. Vyberte testovaciu kazetu zo zataveného fóliového vrecka a spotrebujte ju do 15 minút. Najlepšie výsledky sa dosiahnu, ak sa test vykoná ihneď po otvorení fóliového vrecka.
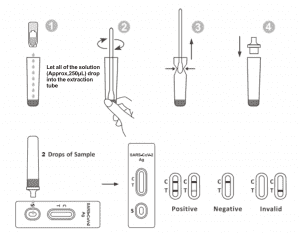
2. Umiestnite extrakčnú skúmavku do pracovnej stanice. Fľašu s extrakčným činidlom držte hore dnom vo zvislej polohe. Stlačte fľašu a nechajte všetok roztok (približne 250 μl) voľne kvapnúť do extrakčnej skúmavky bez toho, aby sa okraj skúmavky dotýkal extrakčnej skúmavky.
3. Vložte vzorku tampónu do extrakčnej skúmavky. Otáčajte tampónom približne 10 sekúnd a zároveň pritláčajte hlavicu k vnútornej strane skúmavky, aby ste uvoľnili antigén z tampónu.
4. Pri vyberaní tampónu stlačte jeho hlavicu smerom k vnútornej strane extrakčnej skúmavky, aby ste z tampónu vytlačili čo najviac tekutiny. Tampón zlikvidujte v súlade s protokolom o likvidácii biologicky nebezpečného odpadu.
5. Nasaďte hrot kvapkadla na vrch extrakčnej skúmavky. Testovaciu kazetu položte na čistý a rovný povrch.
6. Do jamky na vzorku pridajte 2 kvapky roztoku (približne 65 μl) a potom spustite časovač. Zobrazený výsledok odčítajte do 20 – 30 minút a výsledky odčítané po 30 minútach sú neplatné.
INTERPRETÁCIA VÝSLEDKOV
| NEGATÍVNE VÝSLEDOK: |
V kontrolnej oblasti (C) sa objaví jedna farebná čiara. V testovacej oblasti (T) sa neobjaví žiadna čiara. Negatívny výsledok znamená, že antigén SARS-CoV-2 nie je vo vzorke prítomný alebo je prítomný pod detekovateľnou hladinou testu.
POZITÍVNEVÝSLEDOK:
Objavia sa dve čiary. Jedna farebná čiara by mala byť v kontrolnej oblasti (C) a ďalšia zjavná farebná čiara by mala byť v testovacej oblasti (T). Pozitívny výsledok znamená, že vo vzorke bol zistený SARS-CoV-2.
NEPLATNÝ VÝSLEDOK:
Kontrolná čiarka sa neobjavuje. Najpravdepodobnejšími príčinami zlyhania kontrolnej čiarky sú nedostatočný objem vzorky alebo nesprávne postupy. Skontrolujte postup a zopakujte test s novým testom. Ak problém pretrváva, okamžite prestaňte testovaciu súpravu používať a kontaktujte miestneho distribútora.
POZNÁMKA:
Intenzita farby v testovacej oblasti (T) sa bude líšiť v závislosti od koncentrácie antigénu SARS-CoV-2 prítomného vo vzorke. Preto by sa akýkoľvek odtieň farby v testovacej oblasti (T) mal považovať za pozitívny.
KONTROLA KVALITY
- Súčasťou testu je aj procedurálna kontrola. Farebná čiara objavujúca sa v kontrolnej oblasti (C) sa považuje za internú procedurálnu kontrolu. Potvrdzuje dostatočné nasávanie membránou.
- Kontrolné štandardy nie sú súčasťou tejto súpravy; odporúča sa však testovať pozitívne a negatívne kontroly ako správnu laboratórnu prax na potvrdenie testovacieho postupu a overenie správneho vykonania testu.
OBMEDZENIATESTU
- Kazetový rýchly test na antigén SARS-CoV-2 je určený len na profesionálne diagnostické použitie in vitro. Test by sa mal používať na detekciu antigénu SARS-CoV-2 v orofaryngeálnom výtere. Týmto kvalitatívnym testom nie je možné určiť ani kvantitatívnu hodnotu, ani rýchlosť nárastu koncentrácie SARS-CoV-2.
- Presnosť testu závisí od kvality vzorky tampónu. Falošne negatívne výsledky môžu byť výsledkom nesprávneho skladovania odberu vzorky.
- Rýchly test na antigén SARS-CoV-2 v kazete indikuje prítomnosť SARS-CoV-2 iba vo vzorke z životaschopných aj neživotaschopných kmeňov koronavírusu SARS-CoV-2.
- Rovnako ako pri všetkých diagnostických testoch, všetky výsledky sa musia interpretovať spolu s ďalšími klinickými informáciami, ktoré má lekár k dispozícii.
- Negatívny výsledok získaný z tejto súpravy by mal byť potvrdený PCR. Negatívny výsledok sa môže získať, ak koncentrácia SARS-CoV-2 prítomného vo výtere nie je dostatočná alebo je pod detekovateľnou hladinou testu.
- Nadmerné množstvo krvi alebo hlienu na vzorke tampónu môže ovplyvniť výkon a môže viesť k falošne pozitívnemu výsledku.
- Pozitívny výsledok na SARS-CoV-2 nevylučuje základnú koinfekciu s iným patogénom. Preto by sa mala zvážiť možnosť skrytej bakteriálnej infekcie.
- Negatívne výsledky nevylučujú infekciu SARS-CoV-2, najmä u tých, ktorí boli v kontakte s vírusom. Na vylúčenie infekcie u týchto jedincov by sa malo zvážiť následné testovanie molekulárnou diagnostikou.
- Pozitívne výsledky môžu byť spôsobené aktuálnou infekciou kmeňmi koronavírusu inými ako SARS-CoV-2, ako sú koronavírusy HKU1, NL63, OC43 alebo 229E.
- Výsledky antigénových testov by sa nemali používať ako jediný základ pre diagnostiku alebo vylúčenie infekcie SARS-CoV-2 alebo na informovanie o stave infekcie.
- Extrakčné činidlo má schopnosť zabiť vírus, ale nedokáže ho 100 % inaktivovať. Metóda inaktivácie vírusu sa môže riadiť: akú metódu odporúča WHO/CDC, alebo sa s ňou môže zaobchádzať podľa miestnych predpisov.
VÝKONOVÉ CHARAKTERISTIKY
CitlivosťaŠpecifickosť
Rýchlotestovacia kazeta na antigén SARS-CoV-2 bola hodnotená so vzorkami získanými od pacientov. PCR sa používa ako referenčná metóda pre rýchlotestovaciu kazetu na antigén SARS-CoV-2. Vzorky sa považovali za pozitívne, ak PCR preukázala pozitívny výsledok.
| Metóda | RT-PCR | Celkové výsledky | ||
| Rýchlotestovacia kazeta na antigén SARS-CoV-2 | Výsledky | Pozitívny | Negatívne | |
| Pozitívny | 38 | 3 | 41 | |
| Negatívne | 2 | 360 | 362 | |
| Celkové výsledky | 40 | 363 | 403 | |
Relatívna citlivosť: 95,0 % (95 % CI*: 83,1 % – 99,4 %)
Relatívna špecificita: 99,2 % (95 % CI*: 97,6 % – 99,8 %)
*Intervaly spoľahlivosti
Detekčný limit
Keď je obsah vírusu vyšší ako 400 TCID5050/ml, miera pozitívnej detekcie je vyššia ako 95 %. Ak je obsah vírusu nižší ako 200 TCID5050/ml, miera pozitívnej detekcie je nižšia ako 95 %, takže minimálny detekčný limit tohto produktu je 400 TCID50/ml.
Presnosť
Presnosť bola testovaná na tri po sebe idúce šarže činidiel. Rôzne šarže činidiel boli použité na testovanie tej istej negatívnej vzorky 10-krát za sebou a všetky výsledky boli negatívne. Rôzne šarže činidiel boli použité na testovanie tej istej pozitívnej vzorky 10-krát za sebou a všetky výsledky boli pozitívne.
HÁKOVÝ efekt
Keď obsah vírusu v testovanej vzorke dosiahne 4,0*105TCID50/ml, výsledok testu stále nepreukazuje HOOK efekt.
Krížová reaktivita
Bola vyhodnotená skrížená reaktivita súpravy. Výsledky nepreukázali žiadnu skríženú reaktivitu s nasledujúcou vzorkou.
| Meno | Koncentrácia |
| HCOV-HKU1 | 105TCID50/ml |
| Zlatý stafylokok | 106TCID50/ml |
| Streptokoky skupiny A | 106TCID50/ml |
| Vírus osýpok | 105TCID50/ml |
| Vírus mumpsu | 105TCID50/ml |
| Adenovírus typu 3 | 105TCID50/ml |
| Mykoplazmatická pneumónia | 106TCID50/ml |
| Parainfluenzavírus typu 2 | 105TCID50/ml |
| Ľudský metapneumovírus | 105TCID50/ml |
| Ľudský koronavírus OC43 | 105TCID50/ml |
| Ľudský koronavírus 229E | 105TCID50/ml |
| Bordetella parapertusis | 106TCID50/ml |
| Chrípka typu B, kmeň Victoria | 105TCID50/ml |
| Chrípkový kmeň B | 105TCID50/ml |
| Chrípka A H1N1 2009 | 105TCID50/ml |
| Chrípka A H3N2 | 105TCID50/ml |
| H7N9 | 105TCID50/ml |
| H5N1 | 105TCID50/ml |
| Vírus Epstein-Barrovej | 105TCID50/ml |
| Enterovírus CA16 | 105TCID50/ml |
| Rinovírus | 105TCID50/ml |
| Respiračný syncyciálny vírus | 105TCID50/ml |
| Streptococcus pneumoni-ae | 106TCID50/ml |
| Candida albicans | 106TCID50/ml |
| Chlamydia pneumoniae | 106TCID50/ml |
| Bordetella pertussis | 106TCID50/ml |
| Pneumocystis jiroveci | 106TCID50/ml |
| Mycobacterium tuberculosis | 106TCID50/ml |
| Legionella pneumophila | 106TCID50/ml |
Iinterferujúce látky
Výsledky testov nie sú ovplyvnené látkou pri nasledujúcej koncentrácii:
| Rušenie látka | Konc. | Interferujúca látka | Konc. |
| Plná krv | 4% | Zložený benzoínový gél | 1,5 mg/ml |
| Ibuprofén | 1 mg/ml | Kromolynglykát | 15 % |
| tetracyklín | 3 μg/ml | chloramfenikol | 3 μg/ml |
| Mucín | 0,5 % | Mupirocín | 10 mg/ml |
| Erytromycín | 3 μg/ml | Oseltamivir | 5 mg/ml |
| Tobramycín | 5% | Nosové kvapky s nafazolín hydrochloridom | 15 % |
| mentol | 15 % | Sprej s flutikazónpropionátom | 15 % |
| Afrín | 15 % | Deoxyepinefrín hydrochlorid | 15 % |
IBIBLIOGRAFIA
1. Weiss SR, Leibowitz JZ. Patogenéza koronavírusu. Adv Virus Res 2011;81:85-164
2. Cui J, Li F, Shi ZL. Pôvod a vývoj patogénnych koronavírusov. Nat Rev Microbiol 2019;17:181-192.
3. Su S, Wong G, Shi W a kol. Epidemiológia, genetická rekombinácia a patogenéza koronavírusov. TrendsMicrobiol 2016;24:490-502.