Cassetta di test rapidu di l'antigene SARS-CoV-2
Descrizzione corta:
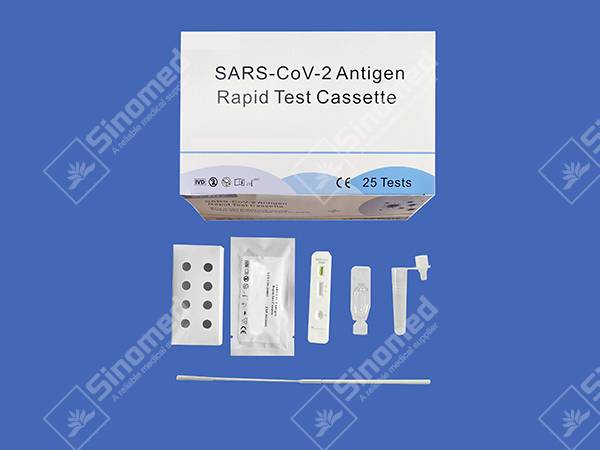
A cassetta di test rapidu di l'antigene SARS-CoV-2 hè un test immunologicu cromatograficu rapidu per a rilevazione qualitativa di l'antigene SARS-CoV-2 in tamponi orofaringei umani. L'identificazione hè basata nantu à l'anticorpi monoclonali specifichi per a proteina nucleocapsidica (N) di SARS-CoV-2. Hè destinata à aiutà in a diagnosi differenziale rapida di l'infezione da COVID-19.
USU PREVISTU
UCassetta di test rapidu di l'antigene SARS-CoV-2hè un test immunologicu cromatograficu rapidu per a rilevazione qualitativa di l'antigenu SARS-CoV-2 in tamponi orofaringei umani. L'identificazione hè basata nantu à l'anticorpi monoclonali specifichi per a proteina nucleocapsidica (N) di SARS-CoV-2. Hè destinatu à aiutà in a diagnosi differenziale rapida diCOVID 19infezzione.
Specifiche di u pacchettu
25 testi/pacchettu, 50 testi/pacchettu, 100 testi/pacchettu
INTRODUZIONE
I novi coronavirus appartenenu à u genaru β.COVID 19hè una malatia infettiva respiratoria acuta. E persone sò generalmente suscettibili. Attualmente, i pazienti infettati da u novu coronavirus sò a principale fonte d'infezzione; e persone infettate asintomatiche ponu ancu esse una fonte infettiva. Basatu annantu à l'attuale investigazione epidemiologica, u periodu d'incubazione hè da 1 à 14 ghjorni, per a maiò parte da 3 à 7 ghjorni. E manifestazioni principali includenu frebba, stanchezza è tosse secca. Congestione nasale, nasu chì cola, mal di gola, mialgia è diarrea si trovanu in pochi casi.
REAGENTI
A cassetta di prova cuntene particelle di proteine nucleocapsidiche anti-SARS-CoV-2 è proteine nucleocapsidiche anti-SARS-CoV-2 rivestite nantu à a membrana.
PRECAUZIONI
Leghjite tutte l'infurmazioni in questu fogliettinu illustrativu prima di fà a prova.
1. Solu per usu diagnosticu prufessiunale in vitro. Ùn aduprà micca dopu a data di scadenza.
2. A prova deve esse mantenuta in a busta sigillata finu à ch'ella sia pronta per esse aduprata.
3. Tutti i campioni devenu esse cunsiderati potenzialmente periculosi è trattati in u listessu modu cum'è un agente infettivu.
4. A prova aduprata deve esse scartata secondu e regulazioni lucali.
5. Evitate d'utilizà campioni sanguinosi.
6. Purtate guanti quandu manighjate i campioni, evitate di toccà a membrana di u reagente è u pozzu di u campione.
CONSERVAZIONE È STABILITÀ
U periodu di validità hè di 18 mesi s'ellu stu pruduttu hè almacenatu in un ambiente di
2-30 ℃. A prova hè stabile finu à a data di scadenza stampata nantu à a busta sigillata. A prova deve stà in a busta sigillata finu à l'usu.ÙN CONGELATE MICCA.Ùn aduprate micca dopu a data di scadenza.
RACCOLTA È PREPARAZIONE DI CAMPIONI
1. Raccolta di secrezioni di gola: Inserite un tampone sterile in gola cumpletamente da a bocca, centrendu nantu à a parete di a gola è a zona arrossata di e tonsille palatine, asciugate e tonsille faringee bilaterali è a parete faringea posteriore cù una pulizia moderata.
forza, evitate di toccà a lingua è cacciate u tampone.
2. Prucessate u campione subitu cù a suluzione d'estrazione di u campione furnita in u kit dopu a raccolta di u campione. S'ellu ùn pò esse trasfurmatu subitu, u campione deve esse cunservatu in un tubu di plastica seccu, sterilizatu è strettamente sigillatu. Pò esse cunservatu à 2-8 ℃ per 8 ore, è pò esse cunservatu per un bellu pezzu à -70 ℃.
3. I campioni chì sò assai contaminati da residui alimentari orali ùn ponu esse aduprati per a prova di stu pruduttu. I campioni raccolti da tamponi chì sò troppu viscosi o agglomerati ùn sò micca cunsigliati per a prova di stu pruduttu. Se i tamponi sò contaminati cù una grande quantità di sangue, ùn sò micca cunsigliati per a prova. Ùn hè micca cunsigliatu di utilizà i campioni chì sò trattati cù una soluzione d'estrazione di campioni micca furnita in questu kit per a prova di stu pruduttu.
COMPONENTI DI U KIT
I materiali furniscenu
| Cassette di prova | Reagente d'estrazione | Tubi d'estrazione | |
| Tamponi sterili | Insertu di u pacchettu | Stazione di travagliu |
Materiali richiesti ma micca furniti
| Cronometru | Per usu di u tempu. |
| Pacchettu |
Specifiche25
testi/pacchettu50
testi/pacchettu 100
testi/pacchettu Reagente d'estrazione di campioni 25 testi/pacchettu 50 testi/pacchettu 100 testi/pacchettu Estrazione di campioni
tubu ≥25 testi/pacchettu ≥50 testi/pacchettu ≥100 testi/pacchettu Istruzzioni Riferitevi à
pacchettu Riferitevi à u
pacchettu Riferitevi à u
pacchettu
ISTRUZIONI PER L'USU
Lasciate chì a prova, u campione, u buffer d'estrazione s'equilibrinu à a temperatura ambiente (15-30 ℃) prima di a prova.
1. Eliminate a cassetta di prova da a busta di foglia d'aluminiu sigillata è adupratela in 15 minuti. I migliori risultati saranu ottenuti se u test hè realizatu subitu dopu l'apertura di a busta di foglia d'aluminiu.
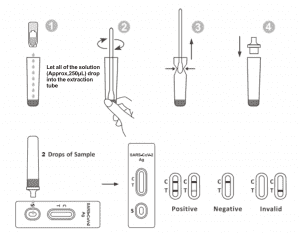
2. Pone u Tubu d'Estrazione in a stazione di travagliu. Tene a buttiglia di reagente d'estrazione à capu in ghjò verticalmente. Stringhje a buttiglia è lasciate chì tutta a suluzione (circa 250 μL) caschi liberamente in u tubu d'estrazione senza toccà u bordu di u tubu à u Tubu d'Estrazione.
3. Pone u campione di tampone in u tubu d'estrazione. Girate u tampone per circa 10 secondi mentre premete a testa contr'à l'internu di u tubu per liberà l'antigenu in u tampone.
4. Eliminate u tampone mentre stringhjite a testa di u tampone contr'à l'internu di u Tubu d'Estrazione mentre u cacciate per espulsà u più liquidu pussibule da u tampone. Scartate u tampone in cunfurmità cù u vostru protocolu di smaltimentu di i rifiuti biologichi.
5. Pone a punta di u contagocce nantu à u tubu d'estrazione. Pone a cassetta di prova nantu à una superficia pulita è piana.
6. Aghjunghjite 2 gocce di a suluzione (circa 65 μL) à u pozzu di u campione è dopu avviate u timer. Leghjite u risultatu visualizatu in 20-30 minuti, è i risultati letti dopu à 30 minuti ùn sò micca validi.
INTERPRETAZIONE DI I RISULTATI
| NEGATIVU RISULTATU: |
Una linea culurata appare in a regione di a linea di cuntrollu (C). Nisuna linea appare in a regione di prova (T). Un risultatu negativu indica chì l'antigenu SARS-CoV-2 ùn hè micca presente in u campione, o hè presente sottu à u livellu rilevabile di a prova.
POSITIVURISULTATU:
Dui linee appariscenu. Una linea culurata deve esse in a regione di cuntrollu (C) è un'altra linea culurata apparente deve esse in a regione di prova (T). Un risultatu pusitivu indica chì u SARS-CoV-2 hè statu rilevatu in u campione.
RISULTATU INVALIDU:
A linea di cuntrollu ùn appare micca. Un vulume insufficiente di campione o tecniche procedurali incorrette sò e ragioni più probabili di fallimentu di a linea di cuntrollu. Rivedite a prucedura è ripetite u test cù un novu test. Se u prublema persiste, smette subitu di utilizà u kit di test è cuntattate u vostru distributore lucale.
NOTA:
L'intensità di u culore in a regione di a linea di prova (T) varierà secondu a cuncentrazione di l'antigene SARS-CoV-2 presente in u campione. Dunque, ogni tonalità di culore in a regione di a linea di prova (T) deve esse cunsiderata positiva.
CONTROLLU DI QUALITÀ
- Un cuntrollu prucedurale hè inclusu in a prova. Una linea culurata chì appare in a regione di cuntrollu (C) hè cunsiderata un cuntrollu prucedurale internu. Cunfirma una assorbimentu adeguatu di a membrana.
- I standard di cuntrollu ùn sò micca furniti cù stu kit; tuttavia, hè cunsigliatu di testà i cuntrolli pusitivi è negativi cum'è una bona pratica di laburatoriu per cunfirmà a prucedura di test è per verificà a prestazione curretta di u test.
LIMITAZIONIDI A PROVA
- A cassetta di test rapidu di l'antigene SARS-CoV-2 hè solu per usu diagnosticu prufessiunale in vitro. U test deve esse adupratu per a rilevazione di l'antigene SARS-CoV-2 in u tampone orofaringeu. Né u valore quantitativu né u tassu di aumentu di a concentrazione di SARS-CoV-2 ponu esse determinati da questu test qualitativu.
- A precisione di a prova dipende da a qualità di u campione di tampone. Falsi negativi ponu risultà da una conservazione impropria di a cullezzione di campioni.
- A cassetta di test rapidu di l'antigene SARS-CoV-2 indicarà solu a presenza di SARS-CoV-2 in u campione da ceppi di coronavirus SARS-CoV-2 viabili è micca viabili.
- Cum'è cù tutti i testi diagnostichi, tutti i risultati devenu esse interpretati inseme cù altre informazioni cliniche dispunibili per u medicu.
- Un risultatu negativu ottenutu da questu kit deve esse cunfirmatu da PCR. Un risultatu negativu pò esse ottenutu se a cuncentrazione di u SARS-CoV-2 presente in u tampone ùn hè micca adatta o hè inferiore à u livellu rilevabile di u test.
- Un eccessu di sangue o di mucus nantu à u campione di tampone pò interferisce cù a prestazione è pò dà un risultatu falsu pusitivu.
- Un risultatu pusitivu per u SARS-CoV-2 ùn esclude micca una coinfezione sottostante cù un altru patogenu. Dunque, a pussibilità di una infezione batterica sottostante deve esse cunsiderata.
- I risultati negativi ùn escludenu micca l'infezzione da SARS-CoV-2, in particulare in quelli chì sò stati in cuntattu cù u virus. I testi di seguitu cù un diagnosticu moleculare devenu esse cunsiderati per escludere l'infezzione in questi individui.
- I risultati pusitivi ponu esse dovuti à una infezione attuale cù ceppi di coronavirus non-SARS-CoV-2, cum'è u coronavirus HKU1, NL63, OC43, o 229E.
- I risultati di i testi di l'antigeni ùn devenu micca esse aduprati cum'è l'unica basa per diagnosticà o escludere l'infezzione da SARS-CoV-2 o per informà u statu di l'infezzione.
- U reagente d'estrazione hà a capacità di tumbà u virus, ma ùn pò micca inattivà u 100% di u virus. U metudu di inattivazione di u virus pò esse riferitu à: quale metudu hè raccomandatu da l'OMS / CDC, o pò esse trattatu secondu e regulazioni lucali.
CARATTERISTICHE DI PRESTAZIONE
SensibilitàèSpecificità
A cassetta di test rapidu di l'antigene SARS-CoV-2 hè stata valutata cù campioni ottenuti da i pazienti. A PCR hè aduprata cum'è metudu di riferimentu per a cassetta di test rapidu di l'antigene SARS-CoV-2. I campioni sò stati cunsiderati pusitivi se a PCR indicava un risultatu pusitivu.
| Metudu | RT-PCR | Risultati Totali | ||
| Cassetta di test rapidu di l'antigene SARS-CoV-2 | Risultati | Positivu | Negativu | |
| Positivu | 38 | 3 | 41 | |
| Negativu | 2 | 360 | 362 | |
| Risultati Totali | 40 | 363 | 403 | |
Sensibilità Relativa: 95,0% (95% CI *: 83,1% - 99,4%)
Specificità Relativa: 99,2% (95% CI *: 97,6%-99,8%)
*Intervalli di fiducia
Limite di rilevazione
Quandu u cuntenutu di virus hè più grande di 400TCID50/ml, u tassu di rilevazione pusitiva hè più grande di 95%. Quandu u cuntenutu di virus hè menu di 200TCID50/ml, u tassu di rilevazione pusitivu hè menu di 95%, dunque u limite minimu di rilevazione di stu pruduttu hè 400TCID50/ml.
Precisione
Trè lotti consecutivi di reagenti sò stati testati per a precisione. Diversi lotti di reagenti sò stati aduprati per testà u listessu campione negativu 10 volte di seguitu, è i risultati eranu tutti negativi. Diversi lotti di reagenti sò stati aduprati per testà u listessu campione pusitivu 10 volte di seguitu, è i risultati eranu tutti pusitivi.
Effettu GANCI
Quandu u cuntenutu di virus in u campione da testà righjunghji 4.0 * 105TCID50/ml, u risultatu di a prova ùn mostra ancu l'effettu HOOK.
Reattività incrociata
A reattività incruciata di u Kit hè stata valutata. I risultati ùn anu mostratu alcuna reattività incruciata cù u campione seguente.
| Nome | Cuncentrazione |
| HCOV-HKU1 | 105TCID50/ml |
| Staphylococcus aureus | 106TCID50/ml |
| Streptococchi di u gruppu A | 106TCID50/ml |
| Virus di u morbillu | 105TCID50/ml |
| Virus di a parotite | 105TCID50/ml |
| Adenovirus di tipu 3 | 105TCID50/ml |
| Pneumonia micoplasmatica | 106TCID50/ml |
| Virus di a parainfluenza, tipu 2 | 105TCID50/ml |
| Metapneumovirus umanu | 105TCID50/ml |
| Coronavirus umanu OC43 | 105TCID50/ml |
| Coronavirus umanu 229E | 105TCID50/ml |
| Bordetella parapertusis | 106TCID50/ml |
| Influenza B Victoria STRAIN | 105TCID50/ml |
| Influenza B YSTRAIN | 105TCID50/ml |
| Influenza A H1N1 2009 | 105TCID50/ml |
| Influenza A H3N2 | 105TCID50/ml |
| H7N9 | 105TCID50/ml |
| H5N1 | 105TCID50/ml |
| Virus di Epstein-Barr | 105TCID50/ml |
| Enterovirus CA16 | 105TCID50/ml |
| Rinovirus | 105TCID50/ml |
| Virus rispiratoriu sincitiali | 105TCID50/ml |
| Streptococcus pneumoni-ae | 106TCID50/ml |
| Candida albicans | 106TCID50/ml |
| Chlamydia pneumoniae | 106TCID50/ml |
| Bordetella pertussis | 106TCID50/ml |
| Pneumocystis jiroveci | 106TCID50/ml |
| Mycobacterium tuberculosis | 106TCID50/ml |
| Legionella pneumophila | 106TCID50/ml |
ISustanze interferenti
I risultati di a prova ùn interferiscenu micca cù a sustanza à a seguente cuncentrazione:
| Interferendu sustanza | Cunc. | Sustanza interferente | Cunc. |
| Sangue Interu | 4% | Gel di Benzoina Cumpostu | 1,5 mg/ml |
| Ibuprofene | 1mg/ml | Glicatu di cromolina | 15% |
| tetraciclina | 3ug/ml | cloramfenicolu | 3ug/ml |
| Mucina | 0,5% | Mupirocina | 10mg/ml |
| Eritromicina | 3ug/ml | Oseltamivir | 5mg/ml |
| Tobramicina | 5% | Gocce nasali di cloridrato di nafazolina | 15% |
| mentolu | 15% | Spray di propionatu di fluticasone | 15% |
| Afrin | 15% | Cloridrato di deossiepinefrina | 15% |
IBLIBLIOGRAFIA
1. Weiss SR, Leibowitz JZ. Patogenesi di u coronavirus. Adv Virus Res 2011;81:85-164
2.Cui J, Li F, Shi ZL.Origine è evoluzione di i coronavirus patogeni.Nat Rev Microbiol 2019;17:181-192.
3.Su S, Wong G, Shi W, et al. Epidemiologia, ricombinazione genetica è patogenesi di i coronavirus. TrendsMicrobiol 2016; 24: 490-502.