Касета хуткага тэсту на антыген SARS-CoV-2
Кароткае апісанне:
Касета для хуткага тэсту на антыген SARS-CoV-2 - гэта хуткі імунахраматаграфічны аналіз для якаснага выяўлення антыгена SARS-CoV-2 у мазках з ротаглоткі чалавека. Ідэнтыфікацыя заснавана на моноклональных антыцелах, спецыфічных для нуклеакапсіднага (N) бялку SARS-CoV-2. Ён прызначаны для дапамогі ў хуткай дыферэнцыяльнай дыягностыцы інфекцыі COVID-19.
ПРЫЗНАЧЭННЕ
ГэтыКасета хуткага тэсту на антыген SARS-CoV-2- гэта хуткі імунахраматаграфічны аналіз для якаснага выяўлення антыгена SARS-CoV-2 у мазках з ротаглоткі чалавека. Ідэнтыфікацыя заснавана на моноклональных антыцелах, спецыфічных для нуклеакапсіднага (N) бялку SARS-CoV-2. Ён прызначаны для садзейнічання хуткай дыферэнцыяльнай дыягностыцы.COVID-19інфекцыя.
Тэхнічныя характарыстыкі пакета
25 тэстаў/ўпакоўка, 50 тэстаў/ўпакоўка, 100 тэстаў/ўпакоўка
УВОДЗІНЫ
Новыя каранавірусы адносяцца да роду β.COVID-19— гэта вострае рэспіраторнае інфекцыйнае захворванне. Людзі, як правіла, успрымальныя да яго. У цяперашні час пацыенты, заражаныя новым каранавірусам, з'яўляюцца асноўнай крыніцай інфекцыі; бессімптомныя інфікаваныя людзі таксама могуць быць крыніцай інфекцыі. Згодна з бягучымі эпідэміялагічнымі даследаваннямі, інкубацыйны перыяд складае ад 1 да 14 дзён, часцей за ўсё ад 3 да 7 дзён. Асноўнымі праявамі з'яўляюцца ліхаманка, стомленасць і сухі кашаль. У некаторых выпадках сустракаюцца заложеннасць носа, насмарк, боль у горле, міалгія і дыярэя.
РЭАГЕНТЫ
Тэставая касета змяшчае часціцы нуклеакапсіду супраць SARS-CoV-2 і нуклеакапсіду супраць SARS-CoV-2, нанесеныя на мембрану.
МЕРЫ ЗАСЦЯРОГІ
Калі ласка, прачытайце ўсю інфармацыю ў гэтым пакеце перад выкананнем тэсту.
1. Толькі для прафесійнай дыягностыкі in vitro. Не выкарыстоўваць пасля заканчэння тэрміну прыдатнасці.
2. Тэст павінен заставацца ў герметычным пакеце да выкарыстання.
3. Усе ўзоры павінны лічыцца патэнцыйна небяспечнымі і апрацоўвацца з імі гэтак жа, як і з узбуджальнікамі інфекцыі.
4. Выкарыстаны тэст павінен быць утылізаваны ў адпаведнасці з мясцовымі правіламі.
5. Пазбягайце выкарыстання ўзораў крыві.
6. Пры працы з узорамі апранайце пальчаткі, пазбягайце дакранацца да мембраны рэагента і лункі для ўзору.
ЗАХОЎВАННЕ І СТАБІЛЬНАСЦЬ
Тэрмін прыдатнасці складае 18 месяцаў, калі гэты прадукт захоўваецца ў асяроддзі
2-30℃. Тэст стабільны да заканчэння тэрміну прыдатнасці, пазначанага на запячатаным пакеце. Тэст павінен заставацца ў запячатаным пакеце да выкарыстання.НЕ ЗАМАРОЖВАЦЬ.Не выкарыстоўвайце пасля заканчэння тэрміну прыдатнасці.
ЗБОР І ПАДРЫХТОЎКА ЎЗОРАЎ
1. Збор сакрэту з горла: увядзіце стэрыльны тампон у горла цалкам з ротавай поласці, цэнтраваўшыся на сценцы горла і пачырванелай вобласці паднябенных міндалін, працярыце двухбаковыя глоточныя міндаліны і заднюю сценку глоткі ўмераным струменем вады.
сілай, не дакранайцеся да языка і дастаньце тампон.
2. Пасля збору ўзору адразу ж апрацуйце яго растворам для экстракцыі ўзору, які ўваходзіць у камплект. Калі яго немагчыма апрацаваць адразу, узор варта захоўваць у сухой, стэрылізаванай і строга запячатанай пластыкавай прабірцы. Яго можна захоўваць пры тэмпературы 2-8℃ на працягу 8 гадзін, а пры тэмпературы -70℃ — працяглы час.
3. Узоры, моцна забруджаныя рэшткамі ежы, не могуць быць выкарыстаны для тэставання гэтага прадукта. Узоры, узятыя з занадта глейкіх або агламераваных тампонаў, не рэкамендуюцца для тэставання гэтага прадукта. Калі тампоны забруджаныя вялікай колькасцю крыві, яны не рэкамендуюцца для тэставання. Не рэкамендуецца выкарыстоўваць для тэставання гэтага прадукта ўзоры, апрацаваныя растворам для экстракцыі ўзораў, які не ўваходзіць у склад гэтага набору.
КАМПАНЕНТЫ КАМПЛЕКТА
Матэрыялы забяспечваюць
| Тэставыя касеты | Экстракцыйны рэагент | Экстракцыйныя трубкі | |
| Стэрыльныя тампоны | Укладыш у камплект | Працоўная станцыя |
Неабходныя матэрыялы, але не прадастаўляюцца
| Таймер | Для выкарыстання ў таймінгу. |
| Пакет |
Тэхнічныя характарыстыкі25
тэсты/упакоўка50
тэсты/упакоўка100
тэстаў/упакоўка Рэагент для экстракцыі ўзораў 25 тэстаў/упакоўка 50 тэстаў/упакоўка 100 тэстаў/упакоўка Экстракцыя ўзораў
трубка≥25 тэстаў/ўпакоўка≥50 тэстаў/ўпакоўка≥100 тэстаў/ўпакоўкаГл. інструкцыю
пакет Глядзіце
пакет Глядзіце
пакет
ІНСТРУКЦЫЯ ПА ВЫКАРЫСТАННІ
Перад тэставаннем дайце тэсту, узору і экстракцыйнаму буферу нагрэцца да пакаёвай тэмпературы (15-30 ℃).
1. Дастаньце тэставую касету з герметычна ўпакаванага пакета і выкарыстоўвайце яе на працягу 15 хвілін. Найлепшыя вынікі будуць атрыманы, калі аналіз будзе праведзены адразу пасля адкрыцця пакета.
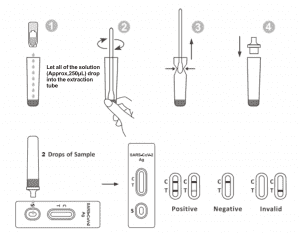
2. Змесціце экстракционную прабірку на працоўную станцыю. Трымайце бутэльку з экстракционным рэагентам вертыкальна дагары нагамі. Сцісніце бутэльку і дайце ўсім растворам (прыблізна 250 мкл) свабодна выліцца ў экстракционную прабірку, не дакранаючыся краю прабіркі да экстракционнай прабіркі.
3. Змесціце ўзор тампона ў прабірку для экстракцыі. Паварочвайце тампон прыблізна 10 секунд, прыціскаючы галоўку да ўнутранай часткі прабіркі, каб вызваліць антыген з тампона.
4. Выміце тампон, прыціскаючы яго галоўку да ўнутранай часткі экстракцыйнай трубкі, каб выціснуць як мага больш вадкасці з тампона. Утылізуйце тампон у адпаведнасці з вашым пратаколам утылізацыі біялагічна небяспечных адходаў.
5. Усталюйце наканечнік піпеткі на верхнюю частку экстракцыйнай трубкі. Змесціце тэставую касету на чыстую і роўную паверхню.
6. Дадайце 2 кроплі раствора (прыблізна 65 мкл) у лунку для ўзору і запусціце таймер. Зчытайце вынік на працягу 20-30 хвілін, вынік, прачытаны пасля 30 хвілін, будзе несапраўдным.
ІНТЭРПРЭТАЦЫЯ ВЫНІКАЎ
| АДМОЎНЫ ВЫНІК: |
У кантрольнай зоне (C) з'яўляецца адна каляровая лінія. У тэставай зоне (T) лініі не з'яўляецца. Адмоўны вынік сведчыць аб тым, што антыген SARS-CoV-2 адсутнічае ва ўзоры або прысутнічае ніжэй за ўзровень выяўлення тэсту.
ПАЗІТЫЎНЫВЫНІК:
З'яўляюцца дзве лініі. Адна каляровая лінія павінна знаходзіцца ў кантрольнай зоне (C), а другая бачная каляровая лінія павінна знаходзіцца ў тэставай зоне (T). Станоўчы вынік сведчыць аб тым, што ва ўзоры быў выяўлены SARS-CoV-2.
НЯДЗЕЙСНЫ ВЫНІК:
Кантрольная лінія не з'яўляецца. Хутчэй за ўсё, прычынай збою кантрольнай лініі з'яўляецца недастатковы аб'ём узору або няправільная працэдура. Праглядзіце працэдуру і паўтарыце тэст з новым тэстам. Калі праблема не знікне, неадкладна спыніце выкарыстанне тэставага набору і звярніцеся да мясцовага дыстрыбутара.
ЗАЎВАГА:
Інтэнсіўнасць колеру ў тэставай зоне (Т) будзе змяняцца ў залежнасці ад канцэнтрацыі антыгена SARS-CoV-2, які прысутнічае ва ўзоры. Таму любы адценне колеру ў тэставай зоне (Т) варта лічыць станоўчым.
КАНТРОЛЬ ЯКАСЦІ
- У тэст уключаны кантрольны этап працэдуры. Каляровая лінія, якая з'яўляецца ў кантрольнай зоне (C), лічыцца ўнутраным кантрольным этапам працэдуры. Гэта пацвярджае адэкватнае ўсмоктванне праз мембрану.
- Кантрольныя стандарты не ўваходзяць у камплект; аднак у адпаведнасці з добрай лабараторнай практыкай рэкамендуецца правесці тэставанне станоўчых і адмоўных кантроляў для пацверджання працэдуры тэставання і праверкі правільнасці правядзення тэсту.
АБМЕЖАВАННІТЭСТ
- Касета хуткага тэсту на антыген SARS-CoV-2 прызначана толькі для прафесійнай дыягностыкі in vitro. Тэст павінен выкарыстоўвацца для выяўлення антыгена SARS-CoV-2 у мазку з ротавай поласці. Гэты якасны тэст не дазваляе вызначыць ні колькаснае значэнне, ні хуткасць павелічэння канцэнтрацыі SARS-CoV-2.
- Дакладнасць тэсту залежыць ад якасці ўзору мазка. Ілжываадмоўныя вынікі могуць быць атрыманы з-за няправільнага захоўвання ўзору.
- Касета хуткага тэсту на антыген SARS-CoV-2 пакажа наяўнасць SARS-CoV-2 толькі ва ўзоры жыццяздольных і нежыццяздольных штамаў каранавіруса SARS-CoV-2.
- Як і ва ўсіх дыягнастычных тэстах, усе вынікі павінны інтэрпрэтавацца разам з іншай клінічнай інфармацыяй, даступнай лекару.
- Адмоўны вынік, атрыманы з дапамогай гэтага набору, павінен быць пацверджаны ПЛР. Адмоўны вынік можа быць атрыманы, калі канцэнтрацыя SARS-CoV-2, які прысутнічае ў мазку, недастатковая або ніжэйшая за ўзровень выяўлення тэсту.
- Лішак крыві або слізі на ўзоры мазка можа паўплываць на прадукцыйнасць і прывесці да ілжыва станоўчага выніку.
- Станоўчы вынік на SARS-CoV-2 не выключае наяўнасці супутняй інфекцыі з іншым узбуджальнікам. Таму варта ўлічваць магчымасць наяўнасці бактэрыяльнай інфекцыі.
- Адмоўныя вынікі не выключаюць інфекцыю SARS-CoV-2, асабліва ў тых, хто кантактаваў з вірусам. Для выключэння інфекцыі ў гэтых асоб варта разгледзець магчымасць наступнага малекулярнага дыягностычнага тэставання.
- Станоўчыя вынікі могуць быць выкліканыя наяўнай інфекцыяй штамамі каранавіруса, не звязанымі з SARS-CoV-2, такімі як каранавірусы HKU1, NL63, OC43 або 229E.
- Вынікі тэставання на антыген не павінны выкарыстоўвацца ў якасці адзінай падставы для дыягностыкі або выключэння інфекцыі SARS-CoV-2 або для інфармавання аб статусе інфекцыі.
- Экстракцыйны рэагент мае здольнасць знішчаць вірус, але ён не можа інактываваць 100% віруса. Метад інактывацыі віруса можна азнаёміцца з рэкамендацыямі СААЗ/CDC, або з мясцовымі правіламі.
ХАРАКТАРЫСТЫКІ ЭФЕКТЫЎНАСЦІ
АдчувальнасцьіСпецыфічнасць
Касета хуткага тэсту на антыген SARS-CoV-2 была ацэненая з выкарыстаннем узораў, атрыманых ад пацыентаў. ПЛР выкарыстоўваецца ў якасці эталоннага метаду для касеты хуткага тэсту на антыген SARS-CoV-2. Узоры лічыліся станоўчымі, калі ПЛР паказвала станоўчы вынік.
| Метад | RT-PCR | Агульныя вынікі | ||
| Касета хуткага тэсту на антыген SARS-CoV-2 | Вынікі | Пазітыўны | Адмоўны | |
| Пазітыўны | 38 | 3 | 41 | |
| Адмоўны | 2 | 360 | 362 | |
| Агульныя вынікі | 40 | 363 | 403 | |
Адносная адчувальнасць: 95,0% (95% ДІ*: 83,1%-99,4%)
Адносная спецыфічнасць: 99,2% (95% ДІ*: 97,6%-99,8%)
*Даверныя інтэрвалы
Мяжа выяўлення
Калі ўтрыманне віруса перавышае 400 TCID5050/мл, узровень станоўчага выяўлення перавышае 95%. Калі ўтрыманне віруса менш за 200TCID5050/мл, узровень выяўлення станоўчых вынікаў меншы за 95%, таму мінімальная мяжа выяўлення гэтага прадукта складае 400TCID50/мл.
Дакладнасць
Тры паслядоўныя партыі рэагентаў былі правераны на дакладнасць. Розныя партыі рэагентаў выкарыстоўваліся для тэставання аднаго і таго ж адмоўнага ўзору 10 разоў запар, і ўсе вынікі былі адмоўнымі. Розныя партыі рэагентаў выкарыстоўваліся для тэставання аднаго і таго ж станоўчага ўзору 10 разоў запар, і ўсе вынікі былі станоўчымі.
Эфект ХУКА
Калі ўтрыманне віруса ў тэставаным узоры дасягне 4,0*105TCID50/мл, вынік тэсту ўсё яшчэ не паказвае эфекту ХУКА.
Перакрыжаваная рэактыўнасць
Была ацэнена перакрыжаваная рэактыўнасць набору. Вынікі не паказалі перакрыжаванай рэактыўнасці з наступным узорам.
| Імя | Канцэнтрацыя |
| HCOV-HKU1 | 105TCID50/мл |
| Залацісты стафілакок | 106TCID50/мл |
| стрэптакокі групы А | 106TCID50/мл |
| Вірус адзёру | 105TCID50/мл |
| Вірус свінкі | 105TCID50/мл |
| Адэнавірус тыпу 3 | 105TCID50/мл |
| Мікаплазменная пнеўманія | 106TCID50/мл |
| Парагрыпавірус, тып 2 | 105TCID50/мл |
| Метапнеўмавірус чалавека | 105TCID50/мл |
| Чалавечы каранавірус OC43 | 105TCID50/мл |
| Каранавірус чалавека 229E | 105TCID50/мл |
| Бардэтэла парапертусіс | 106TCID50/мл |
| ШТАМ ГРЫПУ B, ВІКТОРЫЯ | 105TCID50/мл |
| Штам грыпу B | 105TCID50/мл |
| Грып A H1N1 2009 | 105TCID50/мл |
| Грып A H3N2 | 105TCID50/мл |
| H7N9 | 105TCID50/мл |
| H5N1 | 105TCID50/мл |
| Вірус Эпштэйна-Барра | 105TCID50/мл |
| Энтэравірус CA16 | 105TCID50/мл |
| Рынавірус | 105TCID50/мл |
| Рэспіраторны сінцыцыяльны вірус | 105TCID50/мл |
| Streptococcus pneumoni-ae | 106TCID50/мл |
| Кандыда альбіканс | 106TCID50/мл |
| Хламідійная пнеўманія | 106TCID50/мл |
| Бардэтэла коклюшу | 106TCID50/мл |
| Пнеўмацыстная пнеўмацыста Джыровечы | 106TCID50/мл |
| Мікабактэрыі туберкулёзу | 106TCID50/мл |
| Легіёнела пнеўмафіла | 106TCID50/мл |
Iрэчывы, якія перашкаджаюць
Вынікі выпрабаванняў не будуць паўплываць на наступную канцэнтрацыю рэчыва:
| Перашкаджаючы рэчыва | Канцэнтрацыя | Перашкаджаючае рэчыва | Канцэнтрацыя |
| Цэльная кроў | 4% | Складаны бензаінавы гель | 1,5 мг/мл |
| Ібупрофен | 1 мг/мл | Кромалінглікат | 15% |
| тэтрацыклін | 3 мкг/мл | хларамфенікол | 3 мкг/мл |
| Муцын | 0,5% | Мупірацын | 10 мг/мл |
| Эрытроміцын | 3 мкг/мл | Азельтамівір | 5 мг/мл |
| Табраміцын | 5% | Назальныя кроплі нафазаліна гідрахларыду | 15% |
| ментол | 15% | Спрэй флутыказону прапіянату | 15% |
| Афрын | 15% | Дэаксіэпінефрыну гідрахларыд | 15% |
ІБІБЛІЯГРАФІЯ
1. Вайс С.Р., Лейбовіц Дж.З. Патагенез каранавіруса. Adv Virus Res 2011;81:85-164
2. Цуй Дж., Лі Ф., Шы З. Л. Паходжанне і эвалюцыя патагенных каранавірусаў. Nat Rev Microbiol 2019;17:181-192.
3. Су С., Вонг Г., Шы У. і інш. Эпідэміялогія, генетычная рэкамбінацыя і патагенез каранавірусаў. TrendsMicrobiol 2016;24:490-502.