Kaseta szybkiego testu na antygen SARS-CoV-2
Krótki opis:
Kaseta szybkiego testu antygenu SARS-CoV-2 to szybki chromatograficzny test immunologiczny do jakościowego wykrywania antygenu SARS-CoV-2 w ludzkich wymazach z jamy ustnej i gardła. Identyfikacja opiera się na przeciwciałach monoklonalnych swoistych dla białka nukleokapsydu (N) wirusa SARS- CoV-2.Ma na celu pomoc w szybkiej diagnostyce różnicowej zakażenia CoV-19.
PRZEZNACZENIE
TheKaseta szybkiego testu na antygen SARS-CoV-2to szybki chromatograficzny test immunologiczny do jakościowego wykrywania antygenu SARS-CoV-2 w wymazach z jamy ustnej i gardła człowieka. Identyfikacja opiera się na przeciwciałach monoklonalnych swoistych dla białka nukleokapsydu (N) SARS-CoV-2. Ma na celu pomóc w szybkiej diagnostyki różnicowejCOVID 19infekcja.
Specyfikacje pakietu
25 testów/opakowanie, 50 testów/opakowanie, 100 testów/opakowanie
WSTĘP
Nowe koronawirusy należą do rodzaju β.COVID 19to ostra choroba zakaźna dróg oddechowych. Ludzie są na ogół podatni. Obecnie głównym źródłem infekcji są pacjenci zakażeni nowym koronawirusem. Źródłem infekcji mogą być również osoby zakażone bezobjawowo. Na podstawie bieżącego badania epidemiologicznego okres inkubacji wynosi 1 do 14 dni, przeważnie od 3 do 7 dni.Do głównych objawów zalicza się gorączkę, zmęczenie i suchy kaszel.W kilku przypadkach stwierdza się przekrwienie błony śluzowej nosa, katar, ból gardła, bóle mięśni i biegunkę.
ODCZYNNIKI
Kaseta testowa zawiera cząsteczki białka nukleokapsydu anty-SARS-CoV-2 i białka nukleokapsydu anty-SARS-CoV-2 pokryte membraną.
ŚRODKI OSTROŻNOŚCI
Przed wykonaniem testu proszę przeczytać wszystkie informacje zawarte w tej ulotce dołączonej do opakowania.
1.Wyłącznie do użytku w profesjonalnej diagnostyce in vitro.Nie stosować po upływie terminu ważności.
2.Test powinien pozostać w zamkniętej torebce do czasu użycia.
3.Wszystkie próbki należy uznać za potencjalnie niebezpieczne i należy z nimi postępować w taki sam sposób, jak z czynnikiem infekcyjnym.
4.Zużyty test należy wyrzucić zgodnie z lokalnymi przepisami.
5. Unikaj używania krwawych próbek.
6. Podczas podawania próbek należy nosić rękawiczki, unikać dotykania membrany odczynnika i studzienki próbki.
PRZECHOWYWANIE I STABILNOŚĆ
Okres ważności wynosi 18 miesięcy, jeśli produkt jest przechowywany w środowisku
2-30℃.Test jest stabilny do daty ważności wydrukowanej na zapieczętowanej torebce.Test musi pozostać w zapieczętowanym torebce do czasu użycia.NIE ZAMRAŻAĆ.Nie stosować po upływie terminu ważności.
POBIERANIE I PRZYGOTOWANIE PRÓB
1. Pobranie wydzieliny z gardła: Włożyć sterylny wymaz do gardła całkowicie z jamy ustnej, koncentrując się na ścianie gardła i zaczerwienionym obszarze migdałków podniebiennych, przetrzeć obustronne migdałki gardłowe i tylną ścianę gardła umiarkowanym
należy unikać dotykania języka i wyjąć wacik.
2. Po pobraniu próbki natychmiast poddać ją roztworowi do ekstrakcji próbki znajdującemu się w zestawie.Jeżeli nie ma możliwości natychmiastowej obróbki, próbkę należy przechowywać w suchej, wysterylizowanej i szczelnie zamkniętej probówce plastikowej.Można go przechowywać w temperaturze 2-8 ℃ przez 8 godzin i można go przechowywać przez długi czas w temperaturze -70 ℃.
3. Do badania tego produktu nie można używać próbek silnie zanieczyszczonych resztkami jedzenia z jamy ustnej.Próbki pobrane z wymazów, które są zbyt lepkie lub zbrylone, nie są zalecane do badania tego produktu.Jeżeli wymazy są zanieczyszczone dużą ilością krwi, nie zaleca się ich wykonywania.Nie zaleca się używania do testowania tego produktu próbek przetworzonych roztworem do ekstrakcji próbek, który nie jest zawarty w tym zestawie.
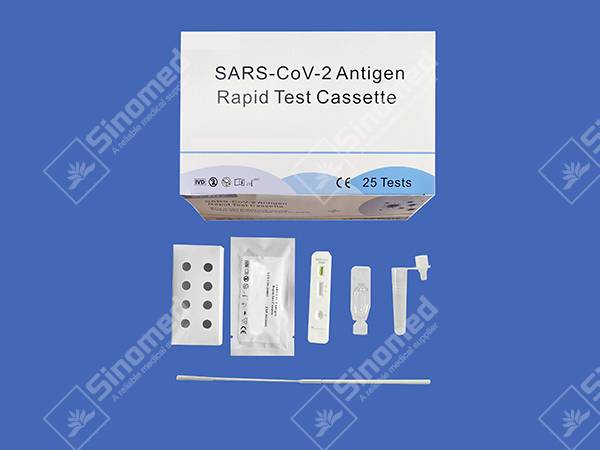
ELEMENTY ZESTAWU
Materiały zapewniają
| Kasety testowe | Odczynnik do ekstrakcji | Rury ekstrakcyjne | |
| Sterylne wymazówki | Ulotka dołączona do opakowania | Stacja robocza |
Materiały wymagane, ale nie zapewniane
| Regulator czasowy | Do użytku w czasie. |
| Pakiet |
Dane techniczne25
testy/opakowanie 50
testy/opakowanie 100
testów/opakowanie Odczynnik do ekstrakcji próbek 25 testów/opakowanie 50 testów/opakowanie 100 testów/opakowanie Ekstrakcja próbek
tuba ≥25 testów/opakowanie ≥50 testów/opakowanie ≥100 testów/opakowanieInstrukcjaPatrz
pakietPatrz
pakietPatrz
pakiet
INSTRUKCJE STOSOWANIA
Przed badaniem poczekaj, aż test, próbka i bufor ekstrakcyjny osiągną temperaturę pokojową (15–30 ℃).
1.Wyjmij kasetę testową z zamkniętej torebki foliowej i zużyj ją w ciągu 15 minut.Najlepsze wyniki uzyska się, jeśli oznaczenie zostanie wykonane natychmiast po otwarciu torebki foliowej.
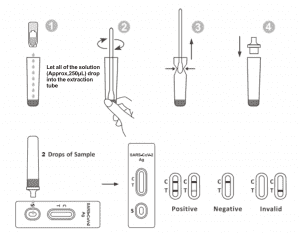
2. Umieść probówkę ekstrakcyjną na stanowisku roboczym. Trzymaj butelkę z odczynnikiem ekstrakcyjnym pionowo do góry dnem. Ściśnij butelkę i pozwól, aby cały roztwór (około 250 μl) spadł do rurki ekstrakcyjnej swobodnie, nie dotykając krawędzi probówki w miejscu ekstrakcji Rura.
3.Umieść wymazówkę w probówce ekstrakcyjnej. Obracaj wymazówkę przez około 10 sekund, jednocześnie dociskając główkę do wnętrza probówki, aby uwolnić antygen z wymazówki.
4. Wyjmij wymazówkę, dociskając główkę wymazówki do wnętrza probówki ekstrakcyjnej podczas jej wyjmowania, aby usunąć z wymazu jak najwięcej płynu. Wymazówkę należy wyrzucić zgodnie z protokołem usuwania odpadów stanowiących zagrożenie biologiczne.
5. Załóż końcówkę zakraplacza na wierzch probówki ekstrakcyjnej. Umieść kasetę testową na czystej i równej powierzchni.
6.Dodaj 2 krople roztworu (około 65μL) do studzienki na próbkę i następnie uruchom stoper.Odczytaj wyświetlony wynik w ciągu 20-30 minut, a wyniki odczytane po 30 minutach są nieważne.
INTERPRETACJA WYNIKÓW
| NEGATYWNY WYNIK: |
W obszarze linii kontrolnej (C) pojawia się jedna kolorowa linia.W obszarze testowym (T) nie pojawia się żadna linia. Wynik ujemny oznacza, że antygen SARS-CoV-2 nie jest obecny w próbce lub jest obecny poniżej wykrywalnego poziomu testu.
POZYTYWNYWYNIK:
Pojawiają się dwie linie. Jedna kolorowa linia powinna znajdować się w obszarze kontrolnym (C), a druga widoczna kolorowa linia powinna znajdować się w obszarze testowym (T). Wynik dodatni wskazuje, że w próbce wykryto SARS-CoV-2.
NIEPRAWIDŁOWY WYNIK:
Linia kontrolna nie pojawia się. Niewystarczająca objętość próbki lub nieprawidłowe techniki proceduralne są najprawdopodobniej przyczyną awarii linii kontrolnej.Przejrzyj procedurę i powtórz test, używając nowego testu.Jeśli problem będzie się powtarzał, natychmiast zaprzestań korzystania z zestawu testowego i skontaktuj się z lokalnym dystrybutorem.
NOTATKA:
Intensywność koloru w obszarze linii testowej (T) będzie się różnić w zależności od stężenia antygenu SARS-CoV-2 obecnego w próbce.Dlatego każdy odcień koloru w obszarze linii testowej (T) należy uznać za pozytywny.
KONTROLA JAKOŚCI
- Badanie obejmuje kontrolę proceduralną.Kolorowa linia pojawiająca się w obszarze kontrolnym (C) jest uznawana za wewnętrzną kontrolę proceduralną. Potwierdza ona odpowiednie odprowadzanie wilgoci przez membranę.
- Standardy kontroli nie są dostarczane z tym zestawem;jednakże zaleca się, aby w ramach dobrej praktyki laboratoryjnej badać kontrole dodatnie i ujemne, aby potwierdzić procedurę testową i sprawdzić prawidłowe działanie testu.
OGRANICZENIATESTU
- TheKaseta szybkiego testu na antygen SARS-CoV-2przeznaczony jest wyłącznie do profesjonalnego użytku w diagnostyce in vitro.Test powinien być stosowany do wykrywania antygenu SARS-CoV-2 w wymazie z jamy ustnej i gardła.Na podstawie tej jakościowej nie można określić ani wartości ilościowej, ani tempa wzrostu stężenia SARS-CoV-2 test.
- Dokładność testu zależy od jakości wymazu. Fałszywie ujemne wyniki mogą wynikać z niewłaściwego przechowywania próbki.
- Kaseta szybkiego testu na antygen SARS-CoV-2 wskaże jedynie obecność SARS-CoV-2 w próbce pochodzącej zarówno z żywych, jak i nieżywotnych szczepów koronaawirusa SARS-CoV-2.
- Podobnie jak w przypadku wszystkich testów diagnostycznych, wszystkie wyniki należy interpretować łącznie z innymi informacjami klinicznymi dostępnymi lekarzowi.
- Wynik ujemny uzyskany z tego zestawu należy potwierdzić metodą PCR. Wynik ujemny można uzyskać w przypadku, gdy stężenie wirusa SARS-CoV-2 w wymazie nie jest odpowiednie lub jest poniżej poziomu wykrywalnego przez test.
- Nadmiar krwi lub śluzu na wymazie może zakłócać działanie i powodować fałszywie dodatni wynik.
- Pozytywny wynik na obecność SARS-CoV-2 nie wyklucza współistniejącej infekcji innym patogenem.Dlatego należy wziąć pod uwagę możliwość infekcji bakteryjnej.
- Ujemne wyniki nie wykluczają zakażenia SARS-CoV-2, zwłaszcza u osób, które miały kontakt z wirusem.Należy rozważyć dalsze badania z diagnostyką molekularną, aby wykluczyć zakażenie u tych osób.
- Pozytywne wyniki mogą być spowodowane obecną infekcją szczepami koronawirusów innymi niż SARS-CoV-2, takimi jak koronawirusy HKU1, NL63, OC43 lub 229E.
- Wyniki badania antygenu nie powinny być wykorzystywane jako jedyna podstawa do diagnozowania lub wykluczania zakażenia SARS-CoV-2 lub do informowania o stanie zakażenia.
- Odczynnik ekstrakcyjny ma zdolność zabijania wirusa, ale nie może inaktywować 100% wirusa. Metodę inaktywacji wirusa można określić: jaka metoda jest zalecana przez WHO/CDC lub można z nią postępować zgodnie z lokalnymi przepisami.
CHARAKTERYSTYKA WYDAJNOŚCI
WrażliwośćISpecyficzność
Kaseta szybkiego testu kasetowego na antygen SARS-CoV-2 została oceniona na podstawie próbek pobranych od pacjentów.PCR jest metodą referencyjną dla kasety szybkiego testu kasetowego na antygen SARS-CoV-2.Próbki uznawano za pozytywne, jeśli PCR wykazał wynik pozytywny.
| metoda | RT-PCR | Wyniki ogółem | ||
| Kaseta szybkiego testu na antygen SARS-CoV-2 | Wyniki | Pozytywny | Negatywny | |
| Pozytywny | 38 | 3 | 41 | |
| Negatywny | 2 | 360 | 362 | |
| Wyniki ogółem | 40 | 363 | 403 | |
Czułość względna: 95,0% (95% CI*: 83,1% -99,4%)
Specyficzność względna: 99,2% (95% CI*: 97,6% -99,8%)
*Przedziały ufności
Granica wykrywalności
Gdy zawartość wirusa jest większa niż 400TCID50/ml, wskaźnik wykrywalności pozytywnej jest większy niż 95%.Gdy zawartość wirusa jest mniejsza niż 200TCID50/ml, wskaźnik wykrywalności pozytywnej jest mniejszy niż 95%, więc minimalny limit wykrywalności tego produktu wynosi 400TCID50/ml.
Precyzja
Trzy kolejne partie odczynników zbadano pod kątem precyzji.Do badania tej samej próbki ujemnej 10 razy z rzędu użyto różnych partii odczynników i wszystkie wyniki były ujemne.Do przetestowania tej samej pozytywnej próbki 10 razy z rzędu użyto różnych partii odczynników i wszystkie wyniki były pozytywne.
Efekt HAKA
Gdy zawartość wirusa w badanej próbce osiągnie 4,0*105TID50/ml, wynik testu w dalszym ciągu nie wykazuje efektu HOOK.
Reaktywność krzyżowa
Oceniono reaktywność krzyżową zestawu.Wyniki nie wykazały reakcji krzyżowej z następującą próbką.
| Nazwa | Stężenie |
| HCOV-HKU1 | 105TID50/ml |
| Staphylococcus aureus | 106TID50/ml |
| Paciorkowce grupy A | 106TID50/ml |
| Wirus odry | 105TID50/ml |
| Wirus świnki | 105TID50/ml |
| Adenowirus typu 3 | 105TID50/ml |
| Mykoplazmalne zapalenie płuc | 106TID50/ml |
| Wirus paraimfluenza, typ 2 | 105TID50/ml |
| Ludzki metapneumowirus | 105TID50/ml |
| Koronawirus ludzki OC43 | 105TID50/ml |
| Ludzki koronawirus 229E | 105TID50/ml |
| Bordetella parapertusis | 106TID50/ml |
| Grypa B Victoria szczep | 105TID50/ml |
| Grypa B YSTRAIN | 105TID50/ml |
| Grypa A H1N1 2009 | 105TID50/ml |
| Grypa AH3N2 | 105TID50/ml |
| H7N9 | 105TID50/ml |
| H5N1 | 105TID50/ml |
| Wirus Epsteina-Barra | 105TID50/ml |
| Enterowirus CA16 | 105TID50/ml |
| Rinowirus | 105TID50/ml |
| Syncytialny wirus oddechowy | 105TID50/ml |
| Streptococcus pneumoni-ae | 106TID50/ml |
| Candida albicans | 106TID50/ml |
| Chlamydia zapalenie płuc | 106TID50/ml |
| Bordetella pertussis | 106TID50/ml |
| Pneumocystis jiroveci | 106TID50/ml |
| Prątek gruźlicy | 106TID50/ml |
| Legionella pneumophila | 106TID50/ml |
ISubstancje zakłócające
Na wyniki badań nie wpływa substancja w stężeniu:
| Wścibski substancja | stęż. | Substancja zakłócająca | stęż. |
| Pełna krew | 4% | Związek benzoesowy w żelu | 1,5 mg/ml |
| Ibuprofen | 1 mg/ml | Glikan kromoliny | 15% |
| tetracyklina | 3 µg/ml | chloramfenikol | 3 µg/ml |
| Mucyna | 0,5% | Mupirocyna | 10 mg/ml |
| Erytromycyna | 3 µg/ml | Oseltamiwir | 5 mg/ml |
| Tobramycyna | 5% | Krople do nosa z chlorowodorkiem nafazoliny | 15% |
| mentol | 15% | Propionian flutykazonu w sprayu | 15% |
| Afrin | 15% | Chlorowodorek dezoksyepinefryny | 15% |
IBIBLIOGRAFIA
1.Weiss SR, Leibowitz JZ. Patogeneza wirusa koronawirusa.Adv Virus Res 2011;81:85-164
2.Cui J,Li F,Shi ZL.Pochodzenie i ewolucja patogennych koronawirusów.Nat Rev Microbiol 2019;17:181-192.
3. Su S, Wong G, Shi W i in. Epidemiologia, rekombinacja genetyczna i patogeneza koronawirusów.TrendyMicrobiol 2016;24:490-502.