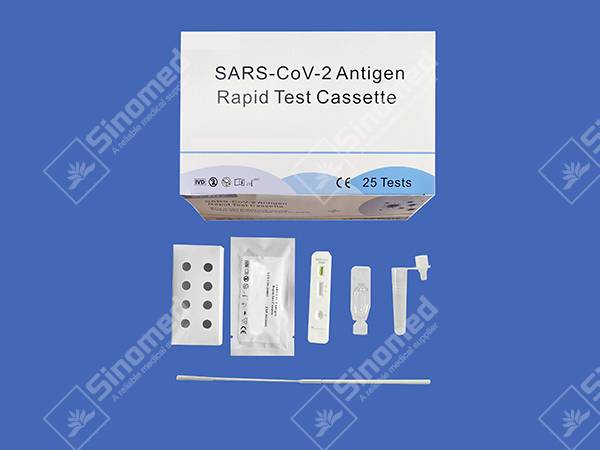
Cassetta per test rapido dell'antigene SARS-CoV-2
Breve descrizione:
La cassetta per test rapido dell'antigene SARS-CoV-2 è un immunodosaggio cromatografico rapido per il rilevamento qualitativo dell'antigene SARS-CoV-2 nei tamponi orofaringei umani. L'identificazione si basa sugli anticorpi monoclonali specifici per la proteina nucleocapside (N) di SARS-CoV-2. È destinato a facilitare la diagnosi differenziale rapida dell'infezione da COVID-19.
USO PREVISTO
ILCassetta per test rapido dell'antigene SARS-CoV-2è un immunodosaggio cromatografico rapido per la rilevazione qualitativa dell'antigene SARS-CoV-2 nei tamponi orofaringei umani. L'identificazione si basa sugli anticorpi monoclonali specifici per la proteina nucleocapside (N) di SARS-CoV-2. È destinato a facilitare la diagnosi differenziale rapida diCOVID 19infezione.
Specifiche del pacchetto
25 test/confezione, 50 test/confezione, 100 test/confezione
INTRODUZIONE
I nuovi coronavirus appartengono al genere β.COVID 19è una malattia infettiva respiratoria acuta. Le persone sono generalmente suscettibili. Attualmente, i pazienti infettati dal nuovo coronavirus sono la principale fonte di infezione; anche le persone infette asintomatiche possono essere una fonte infettiva. Sulla base delle attuali indagini epidemiologiche, il periodo di incubazione è compreso tra 1 e 14 giorni, solitamente tra 3 e 7 giorni. Le principali manifestazioni includono febbre, affaticamento e tosse secca. In alcuni casi si riscontrano congestione nasale, naso che cola, mal di gola, mialgia e diarrea.
REAGENTI
La cassetta di test contiene particelle proteiche del nucleocapside anti-SARS-CoV-2 e la proteina del nucleocapside anti-SARS-CoV-2 rivestita sulla membrana.
PRECAUZIONI
Prima di eseguire il test, leggere attentamente tutte le informazioni contenute nel foglietto illustrativo.
1. Solo per uso diagnostico professionale in vitro. Non utilizzare dopo la data di scadenza.
2. Il test deve rimanere nella busta sigillata fino al momento dell'uso.
3. Tutti i campioni devono essere considerati potenzialmente pericolosi e maneggiati allo stesso modo di un agente infettivo.
4. Il test utilizzato deve essere smaltito secondo le normative locali.
5. Evitare di utilizzare campioni di sangue.
6. Indossare guanti quando si maneggiano i campioni, evitare di toccare la membrana del reagente e il pozzetto del campione.
CONSERVAZIONE E STABILITÀ
Il periodo di validità è di 18 mesi se il prodotto è conservato in un ambiente di
2-30℃. Il test è stabile fino alla data di scadenza stampata sulla busta sigillata. Il test deve rimanere nella busta sigillata fino al momento dell'usoNON CONGELARE.Non utilizzare oltre la data di scadenza.
RACCOLTA E PREPARAZIONE DEI CAMPIONI
1. Raccolta delle secrezioni faringee: inserire un tampone sterile nella gola completamente dalla bocca, centrandosi sulla parete della gola e sulla zona arrossata delle tonsille palatali, pulire le tonsille faringee bilaterali e la parete faringea posteriore con moderata
con forza, evitare di toccare la lingua ed estrarre il tampone.
2. Analizzare immediatamente il campione con la soluzione di estrazione fornita nel kit dopo il prelievo. Se non è possibile analizzarlo immediatamente, conservarlo in una provetta di plastica asciutta, sterilizzata e rigorosamente sigillata. Può essere conservato a una temperatura compresa tra 2 e 8 °C per 8 ore e a una temperatura di -70 °C per un periodo prolungato.
3. I campioni fortemente contaminati da residui di cibo orale non possono essere utilizzati per testare questo prodotto. I campioni raccolti da tamponi troppo viscosi o agglomerati non sono raccomandati per testare questo prodotto. Se i tamponi sono contaminati da una grande quantità di sangue, non sono raccomandati per il test. Si sconsiglia di utilizzare campioni trattati con una soluzione di estrazione del campione non fornita in questo kit per testare questo prodotto.
COMPONENTI DEL KIT
I materiali forniscono
| Cassette di prova | Reagente di estrazione | Tubi di estrazione | |
| Tamponi sterili | Foglietto illustrativo | Postazione di lavoro |
Materiali richiesti ma non forniti
| Timer | Per uso cronometrico. |
| Pacchetto |
Specifiche25
test/pacchetto50
test/pacchetto100
test/confezioneReagente di estrazione del campione25 test/confezione50 test/confezione100 test/confezioneEstrazione del campione
provetta≥25 test/confezione≥50 test/confezione≥100 test/confezioneIstruzioniFare riferimento a
pacchettoFare riferimento al
pacchettoFare riferimento al
pacchetto
MODALITÀ D'USO
Lasciare che il test, il campione e il tampone di estrazione raggiungano la temperatura ambiente (15-30°C) prima di procedere al test.
1. Estrarre la cassetta di test dalla busta di alluminio sigillata e utilizzarla entro 15 minuti. I risultati migliori si otterranno se il test viene eseguito immediatamente dopo l'apertura della busta di alluminio.
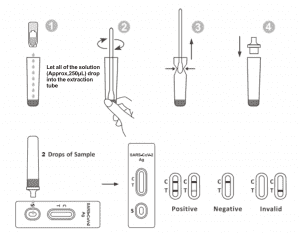
2. Posizionare il tubo di estrazione nella postazione di lavoro. Tenere la bottiglia del reagente di estrazione capovolta in verticale. Premere la bottiglia e lasciare che tutta la soluzione (circa 250 μL) cada liberamente nel tubo di estrazione senza che il bordo del tubo tocchi il tubo di estrazione.
3. Posizionare il campione del tampone nella provetta di estrazione. Ruotare il tampone per circa 10 secondi premendo la testa contro l'interno della provetta per rilasciare l'antigene nel tampone.
4. Rimuovere il tampone premendo la testa del tampone contro l'interno del tubo di estrazione mentre lo si rimuove per espellere quanto più liquido possibile dal tampone. Smaltire il tampone in conformità con il protocollo di smaltimento dei rifiuti biologici pericolosi.
5. Inserire la punta del contagocce sulla parte superiore del tubo di estrazione. Posizionare la cassetta di prova su una superficie pulita e piana.
6. Aggiungere 2 gocce della soluzione (circa 65 μL) nel pozzetto del campione e quindi avviare il timer. Leggere il risultato visualizzato entro 20-30 minuti; i risultati letti dopo 30 minuti non sono validi.
INTERPRETAZIONE DEI RISULTATI
| NEGATIVO RISULTATO: |
Una linea colorata appare nella zona di controllo (C). Nessuna linea appare nella zona del test (T). Un risultato negativo indica che l'antigene SARS-CoV-2 non è presente nel campione o è presente al di sotto del livello rilevabile dal test.
POSITIVORISULTATO:
Compaiono due linee. Una linea colorata dovrebbe trovarsi nella zona di controllo (C) e un'altra linea colorata apparente dovrebbe trovarsi nella zona di test (T). Un risultato positivo indica che il SARS-CoV-2 è stato rilevato nel campione.
RISULTATO NON VALIDO:
La linea di controllo non appare. Un volume di campione insufficiente o tecniche procedurali errate sono le cause più probabili della mancata comparsa della linea di controllo. Rivedere la procedura e ripetere il test con un nuovo test. Se il problema persiste, interrompere immediatamente l'uso del kit e contattare il distributore locale.
NOTA:
L'intensità del colore nella zona della linea di test (T) varia a seconda della concentrazione dell'antigene SARS-CoV-2 presente nel campione. Pertanto, qualsiasi tonalità di colore nella zona della linea di test (T) deve essere considerata positiva.
CONTROLLO QUALITÀ
- Il test include un controllo procedurale. Una linea colorata che compare nella zona di controllo (C) è considerata un controllo procedurale interno. Essa conferma l'adeguata permeabilità della membrana.
- Gli standard di controllo non sono forniti con questo kit; tuttavia, si raccomanda di testare i controlli positivi e negativi come buona pratica di laboratorio per confermare la procedura del test e verificarne la corretta esecuzione.
LIMITAZIONIDEL TEST
- La cassetta per il test rapido dell'antigene SARS-CoV-2 è riservata esclusivamente all'uso diagnostico professionale in vitro. Il test deve essere utilizzato per il rilevamento dell'antigene SARS-CoV-2 nel tampone orofaringeo. Questo test qualitativo non consente di determinare né il valore quantitativo né la velocità di aumento della concentrazione di SARS-CoV-2.
- L'accuratezza del test dipende dalla qualità del campione del tampone. Falsi negativi possono derivare da una conservazione impropria del campione.
- La cassetta per il test rapido dell'antigene SARS-CoV-2 indicherà solo la presenza di SARS-CoV-2 nel campione di ceppi di coronavirus SARS-CoV-2 vitali e non vitali.
- Come per tutti i test diagnostici, tutti i risultati devono essere interpretati insieme alle altre informazioni cliniche a disposizione del medico.
- Un risultato negativo ottenuto da questo kit deve essere confermato tramite PCR. Un risultato negativo può essere ottenuto se la concentrazione del SARS-CoV-2 presente nel tampone non è adeguata o è inferiore al livello rilevabile del test.
- Un eccesso di sangue o muco sul campione del tampone può interferire con le prestazioni e produrre un risultato falso positivo.
- Un risultato positivo per SARS-CoV-2 non esclude una coinfezione sottostante con un altro patogeno. Pertanto, si dovrebbe considerare la possibilità di un'infezione batterica latente.
- I risultati negativi non escludono l'infezione da SARS-CoV-2, in particolare nei soggetti che sono stati in contatto con il virus. Si consiglia di valutare l'esecuzione di test di follow-up con diagnostica molecolare per escludere l'infezione in questi soggetti.
- I risultati positivi potrebbero essere dovuti all'infezione in corso con ceppi di coronavirus non SARS-CoV-2, come i coronavirus HKU1, NL63, OC43 o 229E.
- I risultati dei test antigenici non devono essere utilizzati come unica base per diagnosticare o escludere l'infezione da SARS-CoV-2 o per informare sullo stato dell'infezione.
- Il reagente di estrazione ha la capacità di uccidere il virus, ma non può inattivarlo al 100%. Il metodo di inattivazione del virus può essere consultato: metodo raccomandato dall'OMS/CDC, oppure può essere gestito secondo le normative locali.
CARATTERISTICHE DELLE PRESTAZIONI
SensibilitàESpecificità
La cassetta per il test rapido dell'antigene SARS-CoV-2 è stata valutata con campioni ottenuti dai pazienti. La PCR è utilizzata come metodo di riferimento per la cassetta per il test rapido dell'antigene SARS-CoV-2. I campioni sono stati considerati positivi se la PCR ha indicato un risultato positivo.
| Metodo | RT-PCR | Risultati totali | ||
| Cassetta per test rapido dell'antigene SARS-CoV-2 | Risultati | Positivo | Negativo | |
| Positivo | 38 | 3 | 41 | |
| Negativo | 2 | 360 | 362 | |
| Risultati totali | 40 | 363 | 403 | |
Sensibilità relativa: 95,0% (95%CI*: 83,1%-99,4%)
Specificità relativa: 99,2% (95%CI*: 97,6%-99,8%)
*Intervalli di confidenza
Limite di rilevamento
Quando il contenuto del virus è superiore a 400TCID50/ml, il tasso di rilevamento positivo è superiore al 95%. Quando il contenuto virale è inferiore a 200TCID50/ml, il tasso di rilevamento positivo è inferiore al 95%, quindi il limite minimo di rilevamento di questo prodotto è 400TCID50/ml.
Precisione
Sono stati testati tre lotti consecutivi di reagenti per verificarne la precisione. Diversi lotti di reagenti sono stati utilizzati per testare lo stesso campione negativo 10 volte di seguito, e i risultati sono stati tutti negativi. Diversi lotti di reagenti sono stati utilizzati per testare lo stesso campione positivo 10 volte di seguito, e i risultati sono stati tutti positivi.
Effetto HOOK
Quando il contenuto di virus nel campione da testare raggiunge 4,0*105TCID50/ml, il risultato del test non mostra ancora l'effetto HOOK.
Reattività crociata
È stata valutata la reattività crociata del kit. I risultati non hanno mostrato alcuna reattività crociata con il seguente campione.
| Nome | Concentrazione |
| HCOV-HKU1 | 105TCID50/ml |
| Stafilococco aureo | 106TCID50/ml |
| Streptococchi di gruppo A | 106TCID50/ml |
| Virus del morbillo | 105TCID50/ml |
| Virus della parotite | 105TCID50/ml |
| Adenovirus tipo 3 | 105TCID50/ml |
| Polmonite micoplasmatica | 106TCID50/ml |
| Parainfluenzavirus, tipo 2 | 105TCID50/ml |
| Metapneumovirus umano | 105TCID50/ml |
| Coronavirus umano OC43 | 105TCID50/ml |
| Coronavirus umano 229E | 105TCID50/ml |
| Bordetella parapertusis | 106TCID50/ml |
| Ceppo influenzale B Victoria | 105TCID50/ml |
| Influenza B YSTRAIN | 105TCID50/ml |
| Influenza A H1N1 2009 | 105TCID50/ml |
| Influenza A H3N2 | 105TCID50/ml |
| H7N9 | 105TCID50/ml |
| H5N1 | 105TCID50/ml |
| virus di Epstein-Barr | 105TCID50/ml |
| Enterovirus CA16 | 105TCID50/ml |
| Rinovirus | 105TCID50/ml |
| Virus respiratorio sinciziale | 105TCID50/ml |
| Streptococcus pneumoni-ae | 106TCID50/ml |
| Candida albicans | 106TCID50/ml |
| Chlamydia pneumoniae | 106TCID50/ml |
| Bordetella pertussis | 106TCID50/ml |
| Pneumocystis jiroveci | 106TCID50/ml |
| Mycobacterium tuberculosis | 106TCID50/ml |
| Legionella pneumophila | 106TCID50/ml |
ISostanze interferenti
I risultati del test non subiscono interferenze con la sostanza alla seguente concentrazione:
| Interferire sostanza | Concentrazione | Sostanza interferente | Concentrazione |
| Sangue intero | 4% | Gel di benzoino composto | 1,5 mg/ml |
| Ibuprofene | 1 mg/ml | glicato di cromoglicato | 15% |
| tetraciclina | 3 ug/ml | cloramfenicolo | 3 ug/ml |
| Mucina | 0,5% | Mupirocina | 10 mg/ml |
| Eritromicina | 3 ug/ml | Oseltamivir | 5 mg/ml |
| Tobramicina | 5% | Gocce nasali di nafazolina cloridrato | 15% |
| mentolo | 15% | Spray di propionato di fluticasone | 15% |
| Afrin | 15% | Cloridrato di deossiepinefrina | 15% |
BIBLIOGRAFIA
1.Weiss SR,Leibowitz JZ.Patogenesi del coronavirus. Adv Virus Res 2011;81:85-164
2.Cui J,Li F,Shi ZL.Origine ed evoluzione dei coronavirus patogeni.Nat Rev Microbiol 2019;17:181-192.
3.Su S, Wong G, Shi W, et al. Epidemiologia, ricombinazione genetica e patogenesi dei coronavirus. TrendsMicrobiol 2016; 24: 490-502.