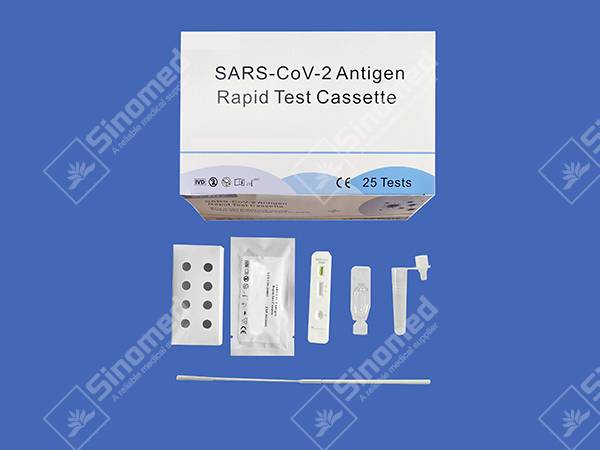
Cassette de test rapide d'antigène SARS-CoV-2
Brève description :
La cassette de test rapide de l'antigène SARS-CoV-2 est un immuno-essai chromatographique rapide pour la détection qualitative de l'antigène SARS-CoV-2 dans les écouvillons oropharyngés humains. L'identification est basée sur les anticorps monoclonaux spécifiques de la protéine de nucléocapside (N) du SARS-CoV-2. Il est destiné à aider au diagnostic différentiel rapide de l'infection au COVID-19.
UTILISATION PRÉVUE
LeCassette de test rapide d'antigène SARS-CoV-2est un dosage immunologique chromatographique rapide pour la détection qualitative de l'antigène du SRAS-CoV-2 dans les écouvillons oropharyngés humains. L'identification est basée sur les anticorps monoclonaux spécifiques de la protéine de nucléocapside (N) du SRAS-CoV-2. Il est destiné à aider au diagnostic différentiel rapide deCOVID 19infection.
Spécifications du package
25 tests/paquet, 50 tests/paquet, 100 tests/paquet
INTRODUCTION
Les nouveaux coronavirus appartiennent au genre β.COVID 19Il s'agit d'une maladie infectieuse respiratoire aiguë. L'homme y est généralement sensible. Actuellement, les patients infectés par le nouveau coronavirus constituent la principale source d'infection ; les personnes infectées asymptomatiques peuvent également être une source d'infection. D'après l'enquête épidémiologique actuelle, la période d'incubation est de 1 à 14 jours, généralement de 3 à 7 jours. Les principales manifestations sont la fièvre, la fatigue et une toux sèche. Une congestion nasale, un écoulement nasal, des maux de gorge, des myalgies et une diarrhée sont observés dans quelques cas.
RÉACTIFS
La cassette de test contient des particules de protéine de nucléocapside anti-SARS-CoV-2 et une protéine de nucléocapside anti-SARS-CoV-2 recouverte sur la membrane.
PRÉCAUTIONS
Veuillez lire toutes les informations contenues dans cette notice avant d’effectuer le test.
1. Réservé à un usage professionnel de diagnostic in vitro. Ne pas utiliser après la date de péremption.
2. Le test doit rester dans la pochette scellée jusqu'à ce qu'il soit prêt à être utilisé.
3. Tous les échantillons doivent être considérés comme potentiellement dangereux et manipulés de la même manière qu’un agent infectieux.
4. Le test utilisé doit être jeté conformément à la réglementation locale.
5. Évitez d’utiliser des échantillons sanglants.
6. Portez des gants lorsque vous manipulez les échantillons, évitez de toucher la membrane du réactif et le puits d'échantillon.
STOCKAGE ET STABILITÉ
La durée de validité est de 18 mois si ce produit est stocké dans un environnement de
2-30℃. Le test est stable jusqu'à la date de péremption imprimée sur la pochette scellée. Le test doit rester dans la pochette scellée jusqu'à utilisation.NE PAS CONGELER.Ne pas utiliser au-delà de la date de péremption.
COLLECTE ET PRÉPARATION DES ÉCHANTILLONS
1. Recueil des sécrétions de la gorge : Insérez un écouvillon stérile dans la gorge complètement depuis la bouche, en centrant sur la paroi de la gorge et la zone rougie des amygdales du palais, essuyez les amygdales pharyngées bilatérales et la paroi pharyngée postérieure avec un chiffon modéré.
forcer, éviter de toucher la langue et retirer l'écouvillon.
2. Après le prélèvement, traiter l'échantillon immédiatement avec la solution d'extraction fournie dans le kit. S'il ne peut être traité immédiatement, conserver l'échantillon dans un tube en plastique sec, stérilisé et hermétiquement fermé. Il peut être conservé à une température comprise entre 2 et 8 °C pendant 8 heures et à -70 °C pendant une longue période.
3. Les échantillons fortement contaminés par des résidus alimentaires oraux ne peuvent pas être utilisés pour tester ce produit. Les échantillons prélevés à partir d'écouvillons trop visqueux ou agglomérés ne sont pas recommandés pour tester ce produit. Si les écouvillons sont contaminés par une quantité importante de sang, ils ne sont pas recommandés pour le test. Il est déconseillé d'utiliser des échantillons traités avec une solution d'extraction non fournie dans ce kit pour tester ce produit.
COMPOSANTS DU KIT
Les matériaux sont fournis
| Cassettes de test | Réactif d'extraction | Tubes d'extraction | |
| écouvillons stériles | Notice d'emballage | Poste de travail |
Matériel requis mais non fourni
| Minuteur | Pour une utilisation chronométrée. |
| Emballer |
Spécifications25
tests/pack50
tests/pack100
tests/packRéactif d'extraction d'échantillons25 tests/pack50 tests/pack100 tests/packExtraction d'échantillons
tube ≥ 25 tests/paquet ≥ 50 tests/paquet ≥ 100 tests/paquet Instructions Se référer à la
packageRéférez-vous au
packageRéférez-vous au
emballer
MODE D'EMPLOI
Laissez le test, l'échantillon et le tampon d'extraction s'équilibrer à température ambiante (15-30℃) avant le test.
1. Retirez la cassette de test de son sachet en aluminium scellé et utilisez-la dans les 15 minutes. Les meilleurs résultats seront obtenus si le test est effectué immédiatement après ouverture du sachet.
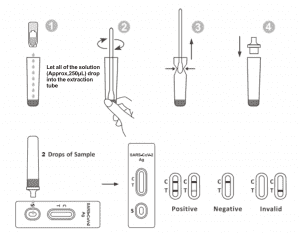
2. Placez le tube d'extraction sur le poste de travail. Tenez le flacon de réactif d'extraction à l'envers verticalement. Pressez le flacon et laissez toute la solution (environ 250 μL) tomber librement dans le tube d'extraction sans toucher le bord du tube au tube d'extraction.
3. Placez l'échantillon d'écouvillon dans le tube d'extraction. Faites tourner l'écouvillon pendant environ 10 secondes tout en appuyant la tête contre l'intérieur du tube pour libérer l'antigène dans l'écouvillon.
4. Retirez l'écouvillon tout en pressant la tête de l'écouvillon contre l'intérieur du tube d'extraction pendant que vous le retirez pour expulser autant de liquide que possible de l'écouvillon. Jetez l'écouvillon conformément à votre protocole d'élimination des déchets biologiques dangereux.
5. Placez l'embout compte-gouttes sur le dessus du tube d'extraction. Placez la cassette de test sur une surface propre et plane.
6. Ajoutez 2 gouttes de la solution (environ 65 μL) dans le puits d'échantillon, puis démarrez le minuteur. Lisez le résultat affiché dans les 20 à 30 minutes, et les résultats lus après 30 minutes ne sont pas valides.
INTERPRÉTATION DES RÉSULTATS
| NÉGATIF RÉSULTAT: |
Une ligne colorée apparaît dans la zone de contrôle (C). Aucune ligne n'apparaît dans la zone de test (T). Un résultat négatif indique que l'antigène du SARS-CoV-2 n'est pas présent dans l'échantillon ou qu'il est présent en dessous du niveau détectable par le test.
POSITIFRÉSULTAT:
Deux lignes apparaissent. Une ligne colorée doit être dans la zone de contrôle (C) et une autre ligne colorée apparente doit être dans la zone de test (T). Un résultat positif indique que le SARS-CoV-2 a été détecté dans l'échantillon.
RÉSULTAT INVALIDE :
La ligne de contrôle n'apparaît pas. Un volume d'échantillon insuffisant ou des techniques de procédure incorrectes sont les causes les plus probables de l'échec de la ligne de contrôle. Revoyez la procédure et répétez le test avec un nouveau test. Si le problème persiste, cessez immédiatement d'utiliser le kit de test et contactez votre distributeur local.
NOTE:
L'intensité de la couleur dans la zone de test (T) varie en fonction de la concentration d'antigène du SARS-CoV-2 présente dans l'échantillon. Par conséquent, toute nuance de couleur dans la zone de test (T) doit être considérée comme positive.
CONTRÔLE DE QUALITÉ
- Un contrôle de procédure est inclus dans le test. Une ligne colorée apparaissant dans la zone témoin (C) est considérée comme un contrôle de procédure interne. Elle confirme une bonne évacuation de la transpiration membranaire.
- Les normes de contrôle ne sont pas fournies avec ce kit ; cependant, il est recommandé de tester les contrôles positifs et négatifs comme bonne pratique de laboratoire pour confirmer la procédure de test et vérifier les performances correctes du test.
LIMITESDU TEST
- La cassette de test rapide de l'antigène SARS-CoV-2 est destinée uniquement à un usage professionnel de diagnostic in vitro. Le test doit être utilisé pour la détection de l'antigène SARS-CoV-2 dans un écouvillon oropharyngé. Ni la valeur quantitative ni le taux d'augmentation de la concentration de SARS-CoV-2 ne peuvent être déterminés par ce test qualitatif.
- La précision du test dépend de la qualité de l'échantillon prélevé. Des faux négatifs peuvent résulter d'un stockage inapproprié de l'échantillon.
- La cassette de test rapide de l'antigène SARS-CoV-2 indiquera uniquement la présence de SARS-CoV-2 dans l'échantillon provenant de souches de coronavirus SARS-CoV-2 viables et non viables.
- Comme pour tous les tests diagnostiques, tous les résultats doivent être interprétés en tenant compte des autres informations cliniques dont dispose le médecin.
- Un résultat négatif obtenu à partir de ce kit doit être confirmé par PCR. Un résultat négatif peut être obtenu si la concentration du SARS-CoV-2 présente dans l'écouvillon n'est pas adéquate ou est inférieure au niveau détectable du test.
- Un excès de sang ou de mucus sur l'échantillon d'écouvillon peut interférer avec les performances et peut donner un résultat faussement positif.
- Un résultat positif au SARS-CoV-2 n'exclut pas une co-infection sous-jacente avec un autre agent pathogène. Par conséquent, la possibilité d'une infection bactérienne sous-jacente doit être envisagée.
- Des résultats négatifs n'excluent pas une infection par le SRAS-CoV-2, en particulier chez les personnes ayant été en contact avec le virus. Un test de suivi avec diagnostic moléculaire doit être envisagé pour exclure une infection chez ces personnes.
- Les résultats positifs peuvent être dus à une infection présente par des souches de coronavirus non-SARS-CoV-2, telles que les coronavirus HKU1, NL63, OC43 ou 229E.
- Les résultats des tests antigéniques ne doivent pas être utilisés comme seule base pour diagnostiquer ou exclure une infection par le SRAS-CoV-2 ou pour informer sur le statut infectieux.
- Le réactif d'extraction a la capacité de tuer le virus, mais il ne peut pas inactiver 100 % du virus. La méthode d'inactivation du virus peut être référencée : quelle méthode est recommandée par l'OMS/CDC, ou elle peut être manipulée conformément aux réglementations locales.
CARACTÉRISTIQUES DE PERFORMANCE
SensibilitéetSpécificité
La cassette de test rapide de l'antigène SARS-CoV-2 a été évaluée avec des échantillons obtenus auprès des patients. La PCR est utilisée comme méthode de référence pour la cassette de test rapide de l'antigène SARS-CoV-2. Les échantillons étaient considérés comme positifs si la PCR indiquait un résultat positif.
| Méthode | RT-PCR | Résultats totaux | ||
| Cassette de test rapide d'antigène SARS-CoV-2 | Résultats | Positif | Négatif | |
| Positif | 38 | 3 | 41 | |
| Négatif | 2 | 360 | 362 | |
| Résultats totaux | 40 | 363 | 403 | |
Sensibilité relative : 95,0 % (IC à 95 %* : 83,1 % - 99,4 %)
Spécificité relative : 99,2 % (IC à 95 %* : 97,6 %-99,8 %)
*Intervalles de confiance
Limite de détection
Lorsque la teneur en virus est supérieure à 400TCID50/ml, le taux de détection positive est supérieur à 95 %. Lorsque la teneur en virus est inférieure à 200 TCID50/ml, le taux de détection positive est inférieur à 95 %, donc la limite de détection minimale de ce produit est de 400 TCID50/ml.
Précision
Trois lots consécutifs de réactifs ont été testés pour en vérifier la précision. Différents lots de réactifs ont été utilisés pour tester le même échantillon négatif dix fois de suite, et les résultats se sont tous révélés négatifs. Différents lots de réactifs ont été utilisés pour tester le même échantillon positif dix fois de suite, et les résultats se sont tous révélés positifs.
Effet HOOK
Lorsque la teneur en virus dans l'échantillon à tester atteint 4,0*105TCID50/ml, le résultat du test ne montre toujours pas l'effet HOOK.
Réactivité croisée
La réactivité croisée du kit a été évaluée. Les résultats n'ont montré aucune réactivité croisée avec l'échantillon suivant.
| Nom | Concentration |
| HCOV-HKU1 | 105TCID50/ml |
| Staphylococcus aureus | 106TCID50/ml |
| streptocoques du groupe A | 106TCID50/ml |
| Virus de la rougeole | 105TCID50/ml |
| Virus des oreillons | 105TCID50/ml |
| Adénovirus de type 3 | 105TCID50/ml |
| Pneumonie à mycoplasmes | 106TCID50/ml |
| Virus para-influenza de type 2 | 105TCID50/ml |
| métapneumovirus humain | 105TCID50/ml |
| Coronavirus humain OC43 | 105TCID50/ml |
| Coronavirus humain 229E | 105TCID50/ml |
| Bordetella parapertusis | 106TCID50/ml |
| Grippe B souche Victoria | 105TCID50/ml |
| SOUCHE B de la grippe | 105TCID50/ml |
| Grippe A H1N1 2009 | 105TCID50/ml |
| Grippe A H3N2 | 105TCID50/ml |
| H7N9 | 105TCID50/ml |
| H5N1 | 105TCID50/ml |
| virus d'Epstein-Barr | 105TCID50/ml |
| Entérovirus CA16 | 105TCID50/ml |
| Rhinovirus | 105TCID50/ml |
| Virus respiratoire syncytial | 105TCID50/ml |
| Streptococcus pneumoni-ae | 106TCID50/ml |
| Candida albicans | 106TCID50/ml |
| Chlamydia pneumoniae | 106TCID50/ml |
| Bordetella pertussis | 106TCID50/ml |
| Pneumocystis jiroveci | 106TCID50/ml |
| Mycobacterium tuberculosis | 106TCID50/ml |
| Legionella pneumophila | 106TCID50/ml |
Isubstances interférentes
Les résultats des tests ne doivent pas être perturbés par la substance à la concentration suivante :
| Interférer substance | Conc. | Substance interférente | Conc. |
| Sang total | 4% | Gel composé de benzoïne | 1,5 mg/ml |
| Ibuprofène | 1 mg/ml | Glycate de cromolyne | 15% |
| tétracycline | 3 ug/ml | chloramphénicol | 3 ug/ml |
| Mucine | 0,5% | Mupirocine | 10 mg/ml |
| Érythromycine | 3 ug/ml | Oseltamivir | 5 mg/ml |
| Tobramycin | 5% | Gouttes nasales à base de chlorhydrate de naphazoline | 15% |
| menthol | 15% | Spray de propionate de fluticasone | 15% |
| Afrin | 15% | Chlorhydrate de désoxyépinéphrine | 15% |
BIBLIOGRAPHIE
1. Weiss SR, Leibowitz JZ. Pathogénèse des coronavirus. Adv Virus Res 2011 ; 81:85-164
2.Cui J,Li F,Shi ZL.Origine et évolution des coronavirus pathogènes.Nat Rev Microbiol 2019;17:181-192.
3. Su S, Wong G, Shi W, et al. Épidémiologie, recombinaison génétique et pathogénèse des coronavirus. TrendsMicrobiol 2016 ; 24 : 490-502.